酰基碳苷是一類(lèi)重要的糖衍生物,因其異頭羰基豐富的反應活性,以及部分含有此類(lèi)骨架的天然產(chǎn)物表現出優(yōu)異的抗氧化活性而備受化學(xué)家關(guān)注(圖1A)。然而,傳統的以金屬試劑為核心的酰基碳苷合成方法往往步驟繁瑣,條件苛刻,且產(chǎn)率低下。近年來(lái),廉價(jià)金屬催化或多途徑協(xié)同催化的策略在酰基碳苷的合成方面已取得重要進(jìn)展(圖1B),但在底物范圍和官能團兼容性方面仍存在一定的局限性,限制了類(lèi)該類(lèi)化合物的后期生物活性開(kāi)發(fā)工作。
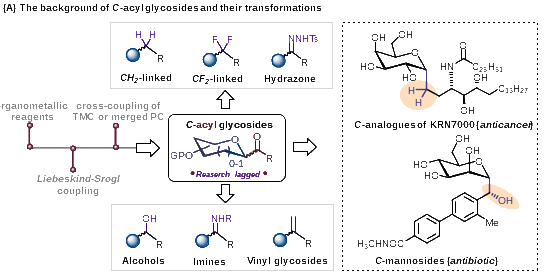
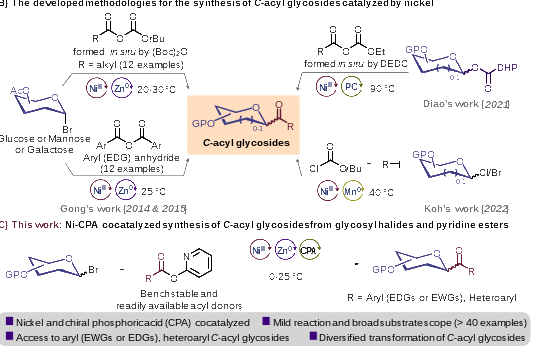
圖1. 酰基碳苷的合成研究進(jìn)展
中國科學(xué)院成都生物研究所馬小鋒課題組在前期工作中,一直致力于溫和條件下多樣化糖苷類(lèi)化合物的合成方法學(xué)研究與生物活性方面的工作(Carbohydr. Res.2023, 108902; Chem. Asian J.2022, 17, e202200120.)。近期,該課題組成功利用鎳催化劑和手性磷酸協(xié)同催化體系,在溫和的反應條件下高效地完成了酰基碳苷的合成。這一新方法不僅顯著(zhù)提高了反應的產(chǎn)率和選擇性,而且突破了已報道方法中對吸電子基團取代的芳基底物和雜芳基底物的限制(圖1C)。
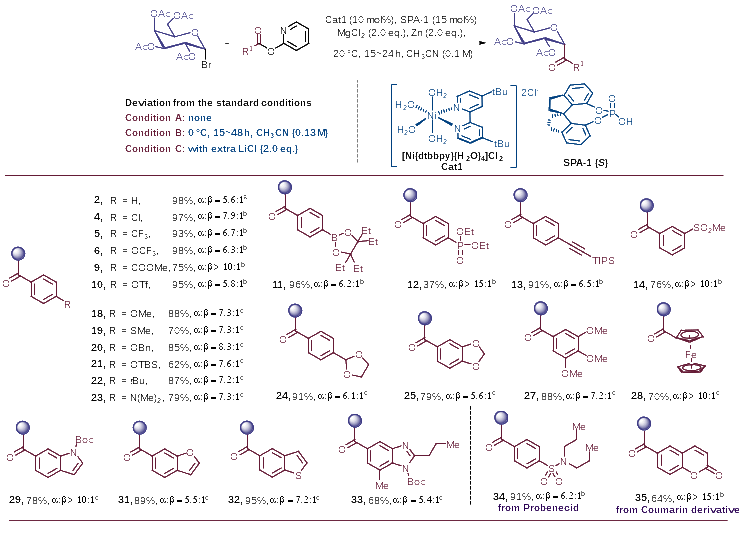
圖2. 底物普適性研究
實(shí)驗中的底物范圍考察結果表明(圖2),該方法適用于不同電子效應基團取代的芳基、雜芳基酰基碳苷的合成,各產(chǎn)物均具有良好的立體選擇性(up to α/β >15:1)以及優(yōu)異的產(chǎn)率(up to 99% yield)。此外,鹵素、酯基、三氟甲磺酸酯、硼酸酯、炔基、醚、二甲氨基、縮醛等官能團以及二茂鐵基在該反應中均具有良好的耐受性。同時(shí),該策略還可用于丙磺舒、香豆素等活性藥物分子的糖基化修飾。為進(jìn)一步證明該方法的普適性,作者還對其他常見(jiàn)的單糖溴代物進(jìn)行了底物拓展(圖3)。葡萄糖、葡醛酸、甘露糖、巖藻糖、鼠李糖的酰基碳苷產(chǎn)物均可通過(guò)該方法順利制備得到。
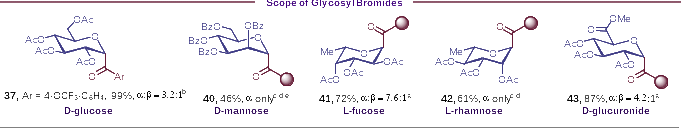
圖3. 底物普適性研究
其次,克級規模放大實(shí)驗進(jìn)一步顯示出該方法具有較高的實(shí)用價(jià)值(圖4)。同時(shí),一系列的轉化實(shí)驗,如將酰基碳苷中的羰基還原為亞甲基或仲醇、與炔丙基溴加成生成含炔基片段的叔醇、與鹽酸羥胺成肟等,也再次印證了酰基碳苷產(chǎn)物多樣性轉化的可行性,為其他復雜碳苷類(lèi)化合物的制備提供了參考依據。
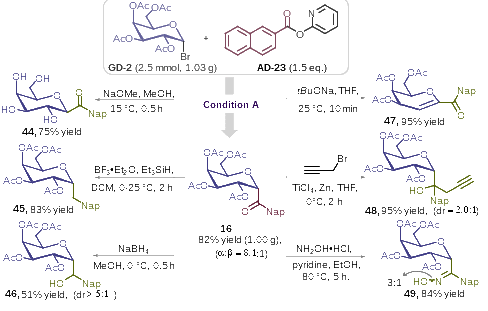
圖4. 合成放大及衍生化研究
最后,初步的自由基捕獲實(shí)驗證明了該反應為鎳催化下的自由基機制(圖4a, 4b)。核磁共振磷譜監測以及紫外-可見(jiàn)光譜分析初步確認了該方法中的手性磷酸可能通過(guò)其雙功能氫鍵作用活化吡啶酯和鎳催化劑(圖4c),進(jìn)而提升反應效率。
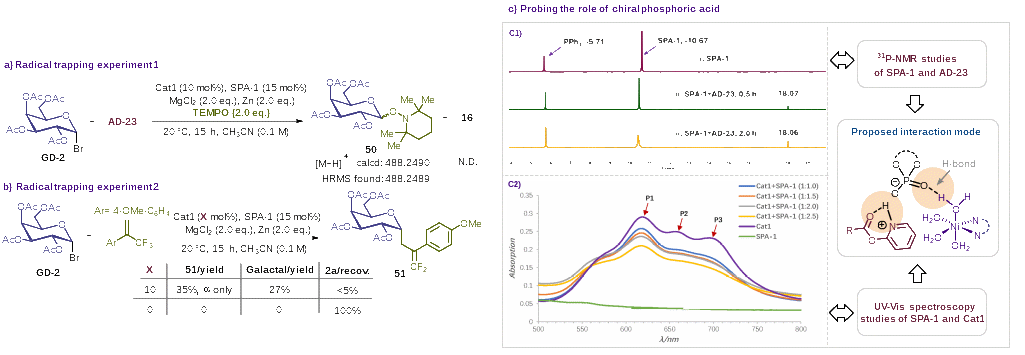
圖4. 初步機理探究
該研究以“Nickel and Chiral Phosphoric Acid Cocatalysis Enables Synthesis of C-Acyl Glycosides發(fā)表于Organic Letters(Org. Lett. 2024, 26, 1332–1337)。中國科學(xué)院成都生物研究所馬小鋒研究員為本文的通訊作者,博士研究生張力為文章第一作者。該研究得到國家自然科學(xué)基金(22377123)、四川省科技計劃項目(2022ZYD0047)、中國科學(xué)院生物資源計劃(KFJBRP-008)的支持。